Проникнув за мембрану клетки, оболочки вируса разрушаются*, а содержимое вирусной частицы смешивается с содержимым цитоплазмы клетки. Дальнейшая стратегическая задача – «перепрошить» генетический материал клетки, интегрировав вирусный геном в геном клетки-хозяина. Однако генетический материал вируса «не в той кодировке» – он в виде РНК, тогда как в ядре клетки-хозяина содержится ДНК. Процесс синтеза и подготовки двухцепочечной спирали ДНК с нити РНК называется обратной транскрипцией. Обратной, так как обычно клетка работает по следующему алгоритму: ДНК → транскрипция в РНК → трансляция РНК в белок, согласно данным с цепочки РНК. А в нашей истории с ВИЧ происходит обратный процесс – вирусная обратная транскриптаза «переписывает» информацию в обратном порядке – с РНК в ДНК.
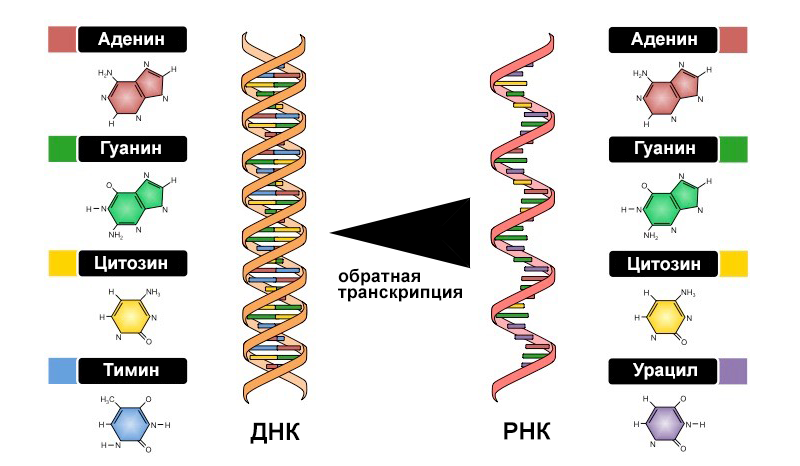
Отметим, что обратная транскриптаза ВИЧ не очень точно работает – считается, что она допускает 5-10 ошибок на 9000 нуклеотидов генома вируса при транскрипции данных, однако, более современные исследования демонстрируют существенную разницу при измерении точности обратной транскриптазы в лабораторных условиях и в живом организме. Установлено, что точность работы обратной транскриптазы очень чувствительна к концентрации ионов магния в клетке и соотношению нуклеозидтрифосфатов и ионов магния в клетке. Вероятно, частота возникновения ошибок в естественных условиях может быть на порядок ниже, чем это считалось ранее. Возникающие мутации в подавляющем числе случаев ухудшают параметры ВИЧ, вплоть до невозможности инфицировать клетки или просто осуществить сборку. Механизмов коррекции ошибок при обратной транскрипции ВИЧ не имеет. Обратная транскрипция – не единственный этап, где могут генерироваться ошибки, но большая часть возникает именно при обратной транскрипции. Не все мутации связаны именно с ошибками копирования – от 20% до 50% являются результатом процесса рекомбинации вирусных РНК.
Многоступенчатый процесс обратной транскрипции умеют «ломать» два широко представленных класса антиретровирусных агентов – НИОТ и ННИОТ.
НИОТ (нуклеозидные ингибиторы обратной транскриптазы), в этот класс объединены нуклеозидные аналоги и нуклеотидные аналоги. С молекулами-аналогами все довольно просто: информация в ДНК записывается всего четырьмя молекулами- «буквами»: тимидин, цитидин, гуанозин и аденозин. «Подменим» их на схожие молекулы лекарств, но без гидроксильной группы, необходимой для образования связей между нуклеотидами, и синтез цепочки ДНК обрывается.
- Аналоги тимидина: зидовудин, ставудин, censavudine (Ed4T);
- Аналоги цитидина: зальцитабин, ламивудин, эмтрицитабин, elvucitabin;
- Аналоги гуанозина: абакавир;
- Аналоги аденозина: диданозин, тенофовир (в т.ч. алафенамид – TAF).
НИОТы, исследования которых были прекращены: amdoxovir, apricitabine, dexelvucitabine, PSI-5004.
Препараты из класса ННИОТ (ненуклеозидные ингибиторы обратной транскриптазы) действуют непосредственно на обратную транскриптазу, связываясь с ней вблизи ее активного центра. Класс представлен следующими препаратами: доравирин, эфавиренз, элсуфавирин, этравирин, fosdevirine, lersivirine, невирапин и рилпивирин.
Viral Decay Accelerators (дословно: ускорители распада вируса) – класс представлен пока только экспериментальной молекулой KP-1461. В организме он метаболизируется до KP-1212, которая в свою очередь является возможным субстратом для обратной транскриптазы вируса, также как аденин, гуанин, тимин и цитозин. Но данная молекула не блокирует транскрипцию, а может осуществлять подмену нуклеотида цитидина или тимидина в синтезируемой цепочке вирусной ДНК, что в результате приводит к возникновению фатальных ошибок в геноме вируса.
Итого: если обратную транскрипцию РНК вируса в ДНК предотвратить не удалось, то в конце этого этапа генетический материал вируса становится готовым для интеграции в ДНК клетки-хозяина. Процессы рекомбинации мы оставляем «за кадром» – для этих процессов пока нет агентов, что могли бы их нарушить, но следует помнить, что генетическое многообразие ВИЧ в том числе обусловлено рекомбинацией двух вирусных РНК, которая тесно связана с обратной транскрипцией.
Так выделены в тексте вышедшие на рынок тех или иных стран препараты, синим выделены препараты, которые находятся в различных стадиях клинических испытаний, и таким цветом обозначены препараты, разработка и исследование которых прекращены.
- Shet A, Nagaraja P, Dixit NM. Viral Decay Dynamics and Mathematical Modeling of Treatment Response: Evidence of Lower in vivo Fitness of HIV-1 Subtype C. J Acquir Immune Defic Syndr. 2016 Nov 1;73(3):245-251. PMID: 27273158.
- Achuthan V, Keith BJ, Connolly BA, DeStefano JJ. Human immunodeficiency virus reverse transcriptase displays dramatically higher fidelity under physiological magnesium conditions in vitro. J Virol. 2014 Aug;88(15):8514-27. PMID: 24850729.
- Preston BD, Poiesz BJ, Loeb LA. Fidelity of HIV-1 reverse transcriptase. Science. 1988 Nov 25;242(4882):1168-71. PMID: 2460924.
- Schlub TE, Grimm AJ, Smyth RP. Fifteen to twenty percent of HIV substitution mutations are associated with recombination. J Virol. 2014 Apr;88(7):3837-49. PMID: 24453357.
- U.S. Department of Health and Human Services (HHS), AIDSinfo.
*Сноска добавлена 13.10.2020. В настоящее время показано, что данное классическое представление, видимо, не является точным. Поскольку интактное ядро ВИЧ-1 слишком велико, чтобы пересечь ядерную пору, счталось, что капсид разрушается перед проникновением ВИЧ-1 в ядро клетки, при чем механизм разрыва капсида «механический» и связан с результатами обратной транскрипции. Подробнеее: Rankovic S, Varadarajan J, Ramalho R, Aiken C, Rousso I. Reverse Transcription Mechanically Initiates HIV-1 Capsid Disassembly. J Virol. 2017 May 26;91(12):e00289-17. PMID: 28381579. В 2020 году быд открыть ядерный эндоцитозоподобный путь, который показал возможность проникновения вириона в ядро «не обращая внимания» на размеры ядерных пор, иным способом. Подробнее: Li X, Wang D, Cui Z, Li Q, Li M, Ma Y, Hu Q, Zhou Y, Zhang XE. HIV-1 viral cores enter the nucleus collectively through the nuclear endocytosis-like pathway. Sci China Life Sci. 2020 May 14. PMID: 32430850.
←Репликационный цикл и точки приложения антиретровирусных агентов. Адсорбция и фузия – Часть II
Репликационный цикл и точки приложения антиретровирусных агентов. Итеграция – Часть IV→
