
Отпущение фармакокинетических грехов? Так не бывает, скажете вы. На самом деле еще как бывает, это вполне научный термин – pharmacokinetic forgiveness, drug forgiveness. Хорошего термина на русском, похоже, не существует, если вы знаете его, то напишите нам. Будем говорить «фармакокинетическое прощение», а греховность мы уже приписали от себя, но в этом есть свой смысл, который мы раскроем ниже.
Антиретровирусные препараты (АРВТ) нужно принимать вовремя. Слишком рано – избыточный уровень препарата и проявления токсичности, или нежелательные (т.е. побочные) явления. Слишком поздно – репликация вируса не подавлена должным образом, а репликация вируса в присутствии недостаточной дозы препарата может оказаться «селекционером», который «выведет» устойчивый к лекарствам штамм вируса и «выбьет» какой-то препарат схемы. Вполне вероятно, что и «выбитый» препарат потянет еще выше вирусную нагрузку, а это, в свою очередь, «выбьет» оставшиеся препараты.
Определение: фармакокинетическое прощение – это время между приемом следующей надлежащей дозой препарата и временем падения до минимальной эффективной концентрации (МЭК/MEC) антиретровирусных препаратов.
Данные о МЭК получают у здоровых добровольцев, которые принимают АРВТ некоторое время, а затем прекращают прием, в это время изучаются концентрации на фоне приема, и те, что будут наблюдаться в «хвосте» после прекращения приема – такие исследования наиболее точны. Можно попытаться получить эти данные, рассуждая о среднем периоде, за которое половина препарата покидает организм, то есть основываясь на периоде полувыведения из стандартных исследований, но это заметно менее точная история, построенная на экстраполяциях.
Кратко о некоторых сложностях: их немало, например, мы иногда говорим о концентрации в плазме, а важна внутриклеточная концентрация, которая может отличаться мало или существенно, как в случае с парой тенофовир дизопропил фумарат и тенофовир алафенамид; мы иногда говорим об одной молекуле препарата, а важны совсем другие, которые получаются после метаболических реакций в организме, как в случае с фосфорилированием НИОТ…
Следует помнить, что наша антиретровирусная терапия – трио или дуэт, второе – если вспомнить и о последних режимах терапии. Функциональная монотерапия, ситуация, когда «сольно» работает только один препарат, – риск возникновения резистентности, то же относится чуть в меньшей мере и к тем случаям, когда фактически работает два препарата из «трио», особенно когда они одного и того же класса.
В таблице ниже представлены данные хвостовых исследований, показывающие долю участников с концентрациями лекарственного средства в плазме ниже предполагаемой МЭК после прекращения приема лекарственного средства (Dickinson L и др., 2015).
| Препарат* | ATV/r | LPV/r | LPV/r x2 | DRV/r |
| Доза, мг | 300/100 | 400/100 | 800/200 | 800/100 |
| МЭК, нг/мл | 150 | 1000 | 1000 | 550 |
| Источник, PMID | 19043924, (21709075) |
19043924 | 19043924 | 21709075 |
| Время, часы | Участники, n/N с концентрацией препарата в плазме ниже МЭК после последнего приема | |||
| 12 | 0/16 | 0/16 | 0/16 | |
| 16 | 0/16 | 2/16 | 0/16 | |
| 20 | 0/16 | 10/16 | 0/16 | |
| 24 | 0/16 | 13/16 | 7/16 | |
| 30 | 2/16 (0/17) | 15/16 | 15/16 | 3/17 |
| 36 | 5 /16 (8/17) | 16/16 | 16/16 | 8/17 |
| 48 | 11/16 (12/17) | 16/16 | 16/16 | 15/17 |
| 60 | 16 /16 (15/17) | 16/16 | 16/16 | 16/16 |
| 72 | 16 /16 | 16/16 | 16/16 | |
| *Один раз в день во всех случаях, кроме LPV/r x2 (Калетра)ATV/r – атазанавир/ритонавир; DRV/r – дарунавир/ритонавир; LPV/r – лопинавир/ритонавир. | ||||
| Препарат | EFV | EVG/COBI | DTG | RPV |
| Доза, мг | 600 | 150/150 | 50 | 25 |
| МЭК, нг/мл | 1000 | 45 | 64 | 50* |
| Источник, PMID | 23274933 | 26679246 | 26679246 | 26195515 |
| Время, часы | Участники, n/N с концентрацией препарата в плазме ниже МЭК после последнего приема | |||
| 24 | 0/17 | 0/17 | 2/18 | |
| 36 | 11/17 | 6/18 | ||
| 48 | 5/16 | 16/17 | 0/17 | 7/18 |
| 60 | 1/17 | |||
| 72 | 1/17 | 11/18 | ||
| 84 | 8/16 | |||
| **МЭК (минимальная эффективная концентрация) определена для рилпивирина недостаточно точно, интерпретировать с осторожностью.DTG – долутегравир; EFV – эфавиренз; EVG/COBI – элвитегравир/кобицистат; RPV – рилпивирин. | ||||
Как мы видим из представленных данных выше, современные «третьи», или «якорные», препараты при дозировании один раз в сутки имеют неплохой потенциал фармакокинетического прощения. Вместе с тем, следует понимать, что имеющиеся данные весьма ограниченные и получены на очень небольших выборках.
Хотя МЭК для НИОТ не установлены, фармакокинетические параметры активных внутриклеточных метаболитов тенофовира и эмтрицитабина были установлены в одном хвостовом исследовании, где было установлено, что оба имеют длительные конечные периоды полувыведения – 164 и 39 часов соответственно.
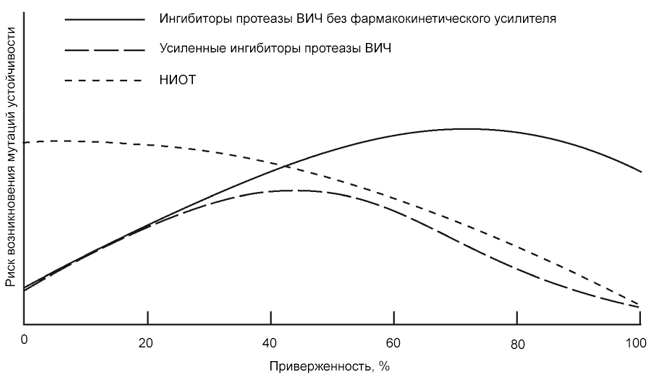 Адаптировано по Bangsberg D.R. и др., 2004. Данная модель иллюстрирует, что у разных классов АРВ-препаратов могут быть весьма различные зависимости рисков формирования резистентности по отношению к приверженности.
Адаптировано по Bangsberg D.R. и др., 2004. Данная модель иллюстрирует, что у разных классов АРВ-препаратов могут быть весьма различные зависимости рисков формирования резистентности по отношению к приверженности.
Другой важный фактор, который нам следует учитывать, – генетический барьер лекарственной устойчивости. К одним препаратам мутации устойчивости возникают с большей вероятностью и за меньшее время, другие препараты «взломать» для ВИЧ значительно сложнее. Значение имеет не только одномоментное наличие вирусной нагрузки и присутствие препарата в концентрации ниже эффективной, но и число мутаций, приводящее к значимой устойчивости.
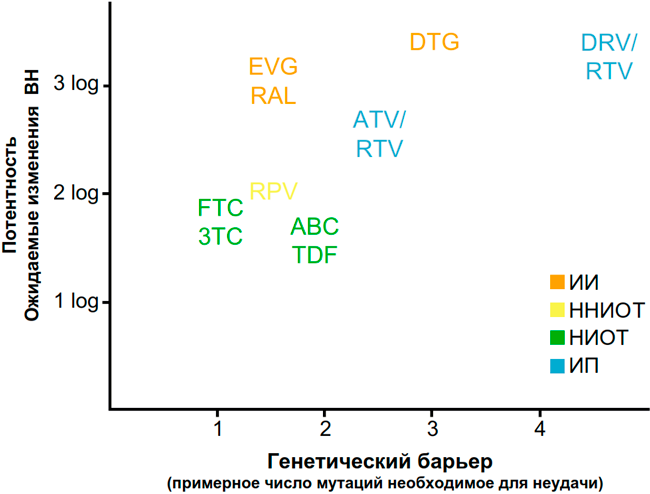 Адаптировано по Clutter D.S. и др., 2016.
Адаптировано по Clutter D.S. и др., 2016.
В любом случае эскадра движется со скоростью самого медленного корабля, а в схеме терапии мы должны в первую очередь думать о слабом звене, о том препарате, что быстрее всех достигнет минимальной эффективной концентрации, а также о том, что имеет более низкий вирусологический барьер.
Пожалуй, наиболее «хрупкий» класс – ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ). Их относительная «хрупкость» складывается из нескольких слагаемых. Они чаще провоцируют на пропуски и прерывания терапии из-за побочных явлений, особенно со стороны центральной нервной системы. Если переносимость не очень хорошая, то она обычно еще и четко связана с приемом препарата, возникая вскоре после, что оказывает дополнительное негативное психологическое давление на пациента. Их действие мощное, но слишком избирательное, механизм воздействия на вирус узок, а значит, и противодействие на узком участке возникнуть может с большей вероятностью. Устойчивость к ННИОТ в значительной мере перекрестная – устойчивость к одному препарату обычно означает устойчивость ко всему классу. Место возникновения мутаций устойчивости в генетическом аппарате вируса находится довольно далеко от консервативных сайтов, где изменения часто губительны для вируса. Длительный период полувыведения дает прощение в случае очень коротких и редких периодов пропусков препарата, но в случае более длительного перерыва в приеме препаратов обуславливает длительные концентрации ниже МЭК, а значит, и риски формирования устойчивого вируса.
В отличие от НИОТ, например, ингибиторы протеазы (ИП) ВИЧ требуют набора мутаций устойчивости, и не все из них могут относиться к лекарственной устойчивости, а иногда направлены на компенсацию изменений, внесенных мутацией устойчивости – оказывается, вирусу не так просто адаптироваться к новым возможностям. Период полувыведения ИП довольно короток, а если препарат скоро покинул организм, то субоптимальные концентрации имели место быть недолго. Мутации к ИП крайне невыгодны для вируса, и при прекращении терапии циркулирующий штамм их довольно быстро теряет, что снижает риски передачи другим людям в виде первичной резистентности.
Полный пропуск терапии
Частота возникновения мутаций устойчивости у людей с подавленной вирусной нагрузкой стремится к нулю. Для изменений уровня вирусной нагрузки нужно некоторое время, а значит, люди со стабильно неопределяемой нагрузкой имеют предельно низкие риски при единичных отклонениях в приверженности. Следствие: – подавленная вирусная нагрузка позволяет одномоментно перенастраивать время приема современной терапии с однократным приемом внутри суток без значимых рисков, естественно, если это происходит лишь изредка; – подавленная вирусная нагрузка практически исключает то, что единичный не систематический полный пропуск терапии повлечет за собой последствия в плане рисков возникновения устойчивости; – упомянутые выше следствия относятся к современным двойным и тройным режимам, но при применении нестандартных режимов, использовании ингибиторов протеазы без бустера, облегченных режимов и монотерапии следует быть предельно осторожным и пунктуальным.
Даже если вирусная нагрузка еще не подавлена ниже уровня 50 РНК ВИЧ копий в мл, справедливым будет утверждать, что единичный полный пропуск терапии, если это не регулярное событие, также не несет никаких измеряемых рисков, во всяком случае в отношении тех случаев, когда применяются стандартные полные и современные режимы терапии с однократным или двукратным приемом.
Как определить, регулярное это событие или нет? Исследования показали, что прием 95% доз препаратов и более не отличается значительно по рискам от приема 100% доз. А значит, высокая приверженность при приеме АРВТ раз в сутки – это пропуск не чаще 1-2 раз в месяц, для приема два раза в сутки – пропуск одного приема не чаще одного случая примерно раз в две недели. Однако приложите все усилия, чтобы иметь 100% приверженность, не стоит сильно полагаться на данные, которые относятся к большим группам.
Потенциал фармакокинетического прощения (Lewis JM и др. 2016)
| Высокий потенциал | Средний потенциал | Низкий потенциал | |||
| Кратность приема | |||||
| Один раз сутки | TDF, ABC, 3TC, FTC, EFV, RPV, ATV/r,DRV/r, EVG/COBI, DTG | LPV/r | |||
| Два раза в сутки | ZDV, LPV/r, RAL, монотерапия DRV/r | монотерапия LPV/r,монотерапия ATV/r,не усиленный ATV | |||
| 3TC–ламивудин; ABC–абакавир; ATV–атазанавир; r–ритонавир; COBI–кобицистат; DRV–дарунавир; DTG–долутегравир; EFV–эфавиренз; EVG–элвитегравир; FTC–эмтрицитабин; RAL–ралтегравир; TDF–тенофовир. | |||||
Прием лишней дозы
Дополнительный прием препаратов возможен при консервативном подходе при смене времени приема режима терапии, но чаще это происходит по той же причине, что и пропуск – забывчивость. Используйте контейнеры для лекарств с ячейками по дням недели, хотя бы записывайте регулярно общее число имеющихся таблеток на определенную дату, чтобы иметь возможность посчитать в случае необходимости.

Принято считать антиретровирусные препараты очень токсичными, однако, тут есть некоторое недопонимание и путаница с разными видами токсичности. Данные о передозировках АРВТ, собранные NPDS (National Poison Data System) в США, говорят о том, что документированных передозировок, в том числе умышленных, происходит в США в год несколько сотен случаев, однако, за период с 2007 по 2011 год лишь одна из более чем 1500 передозировок привела к смерти, тяжелые последствия имели лишь 5 случаев из этих передозировок. Заметим, что в некоторых случаях речь идет о приеме сотен таблеток. Передозировка 270 таблетками Калетры вызывала лишь легкие временные неблагоприятные явления. Однократные дозы 3200 мг дарунавира или 1200 мг атазанавира у здоровых добровольцев не вызывали никаких явных побочных явлений.
Высокие дозы эфавиренза могут у некоторых людей вызывать значимые временные проблемы, связанные с психической деятельностью. Высокие дозы маравирока способны вызвать постуральную гипотензию, то есть падение артериального давления при переходе из сидячего или лежачего положения в положение стоя, что может быть чревато обмороком, падением и травмами.
Таким образом, мы видим, что обычно дополнительный прием одного или всех препаратов вашей схемы терапии не несет никаких измеряемых рисков, за исключением понятных ситуаций с отдельными препаратами, вроде эфавиренза, и то при условии, что препарат переносится именно данным пациентом не идеально. Если по ошибке произошел дополнительный прием препаратов, то не следует предпринимать никаких действий. Время и кратность приема остаются теми же и не требуют никакой коррекции.
Изменение времени приема терапии
Если вы прочитали текст выше, вам уже все ясно. Если ваша терапия - стандартный двойной или тройной режим, смело сдвигайте одномоментно свою терапию на удобное время. Остаетесь вы дома или сменили часовые пояса – не имеет значения. Однако, если вы используете ингибиторы протеазы без усилителя, нестандартные двойные схемы или монотерапию, стоит быть предельно осторожным и производить изменение времени приема мелкими шагами в пределах одного часа каждые сутки.
Заключение
Пунктуальность в приеме препаратов достигается очень просто при правильной организации процесса, и не стоит ей пренебрегать. Следует честно признаться себе в том, что любые поблажки и послабления обычно ведут к другим и еще большим, и в итоге ухудшают приверженность уже критично, к тому же, если это происходит постепенно, то это случается еще и не очень заметно для человека. Все катастрофы – стечение обстоятельств, это относится и к потере вирусологической эффективности режимов АРВТ. Всегда есть некоторые риски наличия или возникновения третьих факторов, в том числе скрытых: полиморфизм системы цитохромов P450 или системы HLA, изменения в параметрах тропности вируса к ко-рецепторам и иной фитнес вируса, некачественный препарат по причинам хранения или брака на производстве, какие-то временные нарушения абсорбции препарата, изменения pH желудочной среды, неучтенные межлекарственные взаимодействия, влияние иных заболеваний… Максимально высокая приверженность достижима, а значит, один фактор всегда в наших, и только в наших руках.
- Lewis JM, Volny-Anne A, Waitt C, Boffito M, Khoo S. Dosing antiretroviral medication when crossing time zones: a review. AIDS. 2016 Jan;30(2):267-71. PMID: 26684823.
- Margolis AM, Heverling H, Pham PA, Stolbach A. A review of the toxicity of HIV medications. J Med Toxicol. 2014 Mar;10(1):26-39. PMID: 23963694.
- Elliot E, Amara A, Jackson A. и др. Dolutegravir and elvitegravir plasma concentrations following cessation of drug intake. J Antimicrob Chemother. 2016 Apr;71(4):1031-6. PMID: 26679246.
- Boffito M, Jackson A, Amara A. и др. Pharmacokinetics of once-daily darunavir-ritonavir and atazanavir-ritonavir over 72 hours following drug cessation. Antimicrob Agents Chemother. 2011 Sep;55(9):4218-23. PMID: 21709075.
- Jackson A, Moyle G, Watson V. и др. Tenofovir, emtricitabine intracellular and plasma, and efavirenz plasma concentration decay following drug intake cessation: implications for HIV treatment and prevention. J Acquir Immune Defic Syndr. 2013 Mar 1;62(3):275-81. PMID: 23274933.
- Dickinson L, Yapa HM, Jackson A. и др. Plasma Tenofovir, Emtricitabine, and Rilpivirine and Intracellular Tenofovir Diphosphate and Emtricitabine Triphosphate Pharmacokinetics following Drug Intake Cessation. 2015 Oct;59(10):6080-6. PMID: 26195515.
- Hermankova M, Ray SC, Ruff C. и др. HIV-1 drug resistance profiles in children and adults with viral load of <50 copies/ml receiving combination therapy. JAMA. 2001 Jul 11;286(2):196-207. PMID: 11448283.
- Bangsberg DR, Moss AR, Deeks SG. Paradoxes of adherence and drug resistance to HIV antiretroviral therapy. J Antimicrob Chemother. 2004 May;53(5):696-9. PMID: 15044425.
- Shuter J. Forgiveness of non-adherence to HIV-1 antiretroviral therapy. J Antimicrob Chemother. 2008 Apr;61(4):769-73. PMID: 18256112.
- Clutter DS, Jordan MR, Bertagnolio S, Shafer RW. HIV-1 drug resistance and resistance testing. Infect Genet Evol. 2016 Dec;46:292-307. PMID: 27587334.
